Induire des anticorps capables de neutraliser le virus malgré sa grande variabilité, telle est la mission que devra remplir le vaccin contre le VIH. Des équipes de recherche du Vaccine Research Center (NIAID) menées par les Drs Kwong et Mascola seraient-ils en passe de trouver la formule miracle ? Leurs travaux très prometteurs, publiés début juin dans la prestigieuse revue Nature Medecine1, ouvrent en tout cas la voie. Ces chercheurs ont basé leur étude sur un nouveau site de vulnérabilité du virus, découvert en 2016 grâce à la caractérisation d’un anticorps neutralisant à large spectre (bNAbs) isolé chez un patient. Situé au niveau du peptide de fusion de la protéine d’enveloppe cet épitope2 reste, au regard de sa fonction indispensable au virus, conservé entre les différentes souches virales. Il agit en effet à une étape très importante du cycle viral, en permettant au virus de se fixer à la surface des cellules cibles. D’après les chercheurs, son rôle primordial et le fait qu’il soit facilement reconnaissable par les anticorps font de ce peptide de fusion un bon candidat vaccin.
Les scientifiques du NIAID3, ont donc conçu plusieurs formulations vaccinales contenant ce peptide de fusion associé à des composés immunogènes4, qu’ils ont testé in vitro et in vivo. Ces différents candidats sont non seulement bien reconnus par les anticorps neutralisants mais ils induisent chez les souris immunisées la production d’anticorps capable de neutraliser 31% des 208 souches virales testées in vitro. Par ailleurs, grâce à l’analyse structurale menée sur ces anticorps, les chercheurs ont optimisé la stratégie d’immunisation utilisée dans le modèle murin. Ils ont ainsi pu déterminer un schéma vaccinal permettant d’induire la production d’anticorps neutralisant à large spectre également chez le cochon d’inde et le macaque rhésus. Les équipes continuent d’optimiser ce candidat vaccin pour le rendre encore plus efficace et espèrent pouvoir lancer des tests chez l’homme très prochainement.
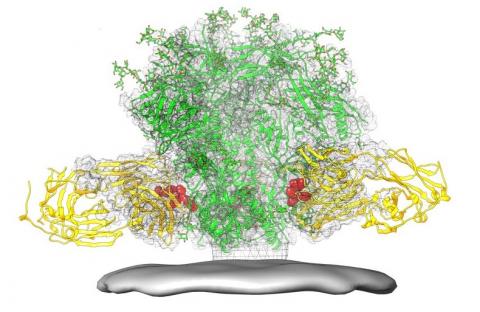
Une nouvelle approche pour identifier des candidats vaccins….
Cette étude montre une fois de plus le rôle primordial des anticorps neutralisant à large spectre dans la lutte contre le virus VIH. Identifiés chez une très faible proportion d’individus infectés, ces anticorps sont capables de neutraliser différentes souches de virus en reconnaissant des zones conservées de la protéine d’enveloppe. A ce jour plus d’une centaine de bNAbs ont été identifiés et grâce aux avancées technologiques, il est aujourd‘hui possible de les produire en grande quantité. Ces anticorps sont d’ailleurs utilisés dans de nombreux essais en thérapie ou en prévention.
L’étude poussée des bNAbs a mis à jour plusieurs sites de vulnérabilité sur le virus, identifiés comme des cibles de choix pour le développement d’un vaccin efficace. Aujourd’hui les chercheurs développent de nouvelles approches de travail5 pour concevoir des vaccins, qui sont basées sur les informations obtenues de la caractérisation de ces anticorps. Une de ces approches, nommée « Epitope-based vaccine design6», consiste à : (1) identifier des anticorps neutralisants à large spectre chez les patients, (2) définir les épitopes viraux qu’ils reconnaissent, (3) concevoir différentes formulations contenant l’épitope en question associé à des composés immunogènes, (4) tester la capacité de ces formulations à induire la production de bNAbs dans des modèles animaux. Cette méthode a été utilisée pour tenter de produire des candidats vaccin contre deux sites de vulnérabilité ; le site de liaison au récepteur CD4 ou le site glycan-V3. Malheureusement, il a été impossible de produire des anticorps neutralisants à large spectre avec ces épitopes pourtant reconnus par des bNAbs. Ces échecs montrent qu’il est souvent difficile de reproduire ce qui peut se passer naturellement.
Néanmoins, la découverte du peptide de fusion a remis les dés en jeu. Les équipes du NIAID à l’origine des travaux publiés dans Nature Medecine ont utilisé cette approche avec succès pour leur étude. Il reste néanmoins de nombreuses interrogations auxquelles les chercheurs devront répondre avant d’arriver à la conception d’un vaccin efficace. Quelle amplitude de neutralisation cette approche peut-elle atteindre ? Les premiers résultats tendent vers une amplitude inférieure à 50%, mais pour être réellement efficace celle-ci doit être plus élevée. De plus la capacité de neutralisation des anticorps produit après immunisation n’a été testée qu’in vitro. La prochaine étape consistera à prouver cette capacité de neutralisation in vivo avec des expériences de challenge7 sur des modèles animaux. Enfin, les bNAbs dirigés contre le peptide de fusion sont présent en faible quantité chez les patients. Or le vaccin devra être en capacité d’en induire une plus grande quantité. Dans ce cas, faudra-t-il utiliser d’autres approches (utilisation de nanoparticules par exemple) pour augmenter l’ampleur de la réponse anticorps induite, si celle-ci se révèle faible ? Ces recherches n’en sont peut-être qu’à leurs prémices, mais elles explorent une stratégie novatrice pour la découverte d’un vaccin efficace contre le VIH.
1- https://www.nature.com/articles/s41591-018-0042-6
2- C’est la partie qui est reconnue par les anticorps
3- NIAID : National Institute of Allergy and Infectious Diseases
4- Composés qui permettent d’induire une réponse immunitaire plus forte
5- https://www.cell.com/immunity/fulltext/S1074-7613(18)30200-0
6- Conception d’un vaccin basé sur les épitopes
7- Ces expériences permettent de tester l’efficacité d’un vaccin à protéger de l’infection. Après avoir reçu une injection du composé vaccinal, les animaux sont exposés au pathogène pour vérifier que le vaccin est capable d’induire une réponse immunitaire protectrice.
 Un pas de plus dans la recherche d’un vaccin contre le VIH
Un pas de plus dans la recherche d’un vaccin contre le VIH